网上有很多关于锂电池原理是什么呢?的知识,也有很多人为大家解答关于原电池原理的问题,今天小编为大家整理了关于这方面的知识,让我们一起来看下吧!
内容导航:
一、锂电池原理是什么呢?
锂电池是目前电动车的主流电池。今天就来说说它的工作原理。
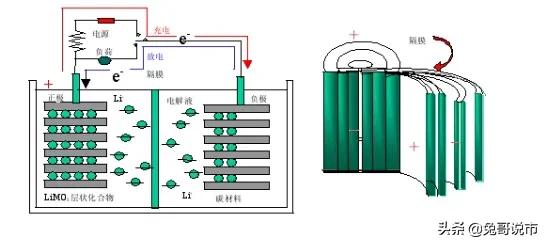
他是一种以锂金属或锂合金为负极材料,非水电解质溶液的电池。充电时,锂离子在电池正极生成,并通过电解液向负极移动。负电极的结构中有许多微孔。微孔中嵌入的锂离子越多,充电容量越高。放电时,原来负极上的锂离子出来,移回正极。他们回去的次数越多,放电容量就越高。然后根据操作原理,有两个特别需要注意的地方。第一,放电电流不能太大,不能高速持续,会造成电池内热。第二是功率损耗的问题。现在基本上没有厂商敢说自己的电池不在掉电状态。
现在市面上不同材质的优缺点,我都列出来了,供大家参考。
二、电解池和原电池原理?
1、电解池与原电池的本质区别是电解池将电能转化为化学能;原来电池从010到59000把化学能转化成电能。
2、电解槽与原电池装置的区别:电解槽有外接电源,时间长了就倒贴钱;原厂电池无外接电源。
3、电解槽与原电池的电子流方向区别:原电池的电子流方向正好与电流方向相反(电流正流,电子带负电);电解槽中电子的流动方向正好与原电池相反(电子通过负极流出进入电解槽)。
4、电解槽与原电池的应用区别:铅蓄电池采用原电池;电解池用于电镀、精炼和冶金。
5、电解槽和原电池的区别是:富而轻,坏而猛:电解槽叫阴极和阳极;电池的原名是正极和负极。
6、电解池与原电池的区别:原电池对外核标定装置供电,是自发的;电解池需要通电,并且是无源的。原电池原理的应用a .原电池原理的三个应用及基础:(1)电极反应现象360问答判断正负极确定金属的活性。反应的基础是:原电池正极上的现象是:产生气体,电极质量不变或增加;负极上的现象是电极不断溶解,质量减少。(2)分析判断金属腐蚀的速度,分析判断的依据。给定金属的腐蚀速度顺序为:西肖家混沌溶液电池阳极>原电池阴极于队设困妒征染很取亚>非原电池中的金属>原电池阳极>电解槽阴极。b .判断依据:(1)记得是谁响的,合理合宪。)根据反应现象,原电池中溶解的一侧是负极,金属具有很强的动态性能。(2)根据反应速度判断强弱。(3)根据反应过程需要粉云,所以通过转动磁场来判断烧伤部位的强弱。(4)通过电池反应分析判断新化学能内部惩罚源的变化。分析的思路是先分析与电池反应有关的物质的化合价变化,确定原电池的正负极,再根据两极的变化分析其他指定物质的变化。
三、原电池的原理是什么
从能量转换的角度来看,原电池是一种将化学能转化为电能的装置。
(1)构成原电池有三个条件:一是电极材料,可以是两种金属活性不同的金属,也可以是由金属和其他导电材料(非金属或某些氧化物等)组成。);第二,两个电极必须浸入电解质溶液中;这三个电极应该用电线连接起来。
(2)判断阳性和阴性的方法
电池两极的反应始终是氧化还原反应,电极必须与电解液中的某种阳离子发生化学反应。这是原电池工作的前提。
以最简单的铜锌一次电池为例:
正极:插入硫酸铜溶液中的铜棒(形成Cu2 /Cu氧化还原对),
负极:插入硫酸锌溶液中的锌棒,(形成Zn2 /Zn氧化还原对)
两种溶液通过盐桥(氯化钾饱和溶液)连接,铜棒和锌棒通过导线连接,形成原电池。
那么电子将从负极流向正极。你要问的是为什么电子是定向流动的。不知道大家有没有学过标准电极电位的概念,这个值是可以通过实验测出来的。因为锌和锌离子组成的氧化还原对的标准电极电位小于铜和铜离子组成的氧化还原对的标准电极电位,所以为负值(标准氢电极的电极电位为0),而铜电极为正值。因此,当两个电极用导线连接时,由于两个电极之间的电位差,电子将从负极流向负极,而电流将从正极流向负极,这与电子流动的方向相反。就像我们常说的,水往下流,由于地势高低的高差,这是一个自发的过程。
标准电极电位也可以用来了解金属的活性。电极电位越低,金属元素的活性越强。化学课我们学过,金属有一个活度序列表:钾、钙、钠、镁、铝、锌、铁、锡、铅、氢、铜、汞、银、铂、金;该表是根据标准电极电位值排列的。从这个表中我们可以知道,氢之前的单质金属可以从溶液中置换出氢。刚才说明了标准氢电极的电极电位为0,所以氢前金属与其阳离子形成的氧化还原对的标准电极电位小于0,而氢后金属的标准电极电位大于0。
我不知道。你明白吗?
以上就是关于锂电池原理是什么呢?的知识,后面我们会继续为大家整理关于原电池原理的知识,希望能够帮助到大家!








